量子化学分子モデリング(DFT/MM)に基づく検証-1
量子化学分子モデリング(DFT/MM)に基づく検証-1
ヒドロキシルラジカルによるミトコンドリア脂質2分子膜の損傷・破壊とそのの検証
- 生体細胞のためミトコンドリア(mt)で発生する最初のエネルギー分子は、活性酸素と呼ばれる水和スーパーオキサイドアニオンラジカル[O2.-(H2O)2]です。それは水和3重項酸素[3O2(H2O)2]がD-グルコースによって還元されて生成します(資料1)。
- 活性酸素[O2.-(H2O)2]はエネルギー物質ATPを生産する一方、細胞内に過酸化水素[HOOH(H2O)2]を副生します(資料2)。
- 活性酸素[O2.-(H2O)2]はHOOHを還元すると、悪玉活性酸と呼ばれるヒドロキシルラジカル[HO.(H2O)2]を与えます(資料3)。活性酸素[O2.-(H2O)2]が運動不足等で細胞内でATP生産等に消費されない場合に起こります。
- ヒドロキシルラジカル[HO.(H2O)2]は、mtの脂質二分子膜を破壊してmtの細胞エネルギー(物質ATPと電磁波エネルギー)の生産と消費の代謝サイクルを狂わせる結果、細胞機能を損わせ、気力、知力、健康力を害わせます(資料4)。
ヨウ化物イオンのミトコンドリア脂質2分子膜に対する優れた抗酸化力の検証
- ヨウ素オメガ3成分のヨウ化物イオンは、細胞内では水和ヨウ化ヒドロにウム[I–OH3+(H2O)]として存在します(資料5)。
- 水和ヨウ化ヒドロニウム[I–OH3+(H2O)]は過酸化水素[HOOH(H2O)2]と会合することでその酸化力を低下させて、HOOHからのヒドロキシルラジカル[HO.(H2O)2]の発生を停止させます。さらにまた、ヨウ化物イオン[I–OH3+(H2O)]は、[HO.(H2O)2]と会合してその酸化分解力を低下させ、mt膜の予防的抗酸化力付与に寄与します(資料6)。
- ヨウ化物イオン[I–OH3+]によってその反応性を失活したラジカル[I–OH3+HO.] は、もはやmt膜を破壊できないことは、DFT/MMによって検証されました(資料7)。
- ヨウ化物イオン[I–OH3+(H2O)]は、オメガ3脂肪酸と会合することで血流に乗って細胞内mtに輸送され、mt膜に吸着することで予防的抗酸化剤となります(資料8)。
- ヨウ化イオン[I–OH3+]の過酸化水素[HOOH(H2O)2]とヒドロキシルラジカル[HO.(H2O)2]それぞれとの反応熱を求め、ビタミンC、A、Eそれぞれの反応熱と比較した。ヨウ化物イオンはビタミンC、A、Eに勝る抗酸化効果を持つことが検証・予見できた(資料9)。
※密度半関数理論(DFT)に基づく分子モデリングのことをですので、以後DFT/MMと表現します。詳しくは、websiteで小生名、Shozo Yanagida, DFT, Mitochondriaで検索ください。
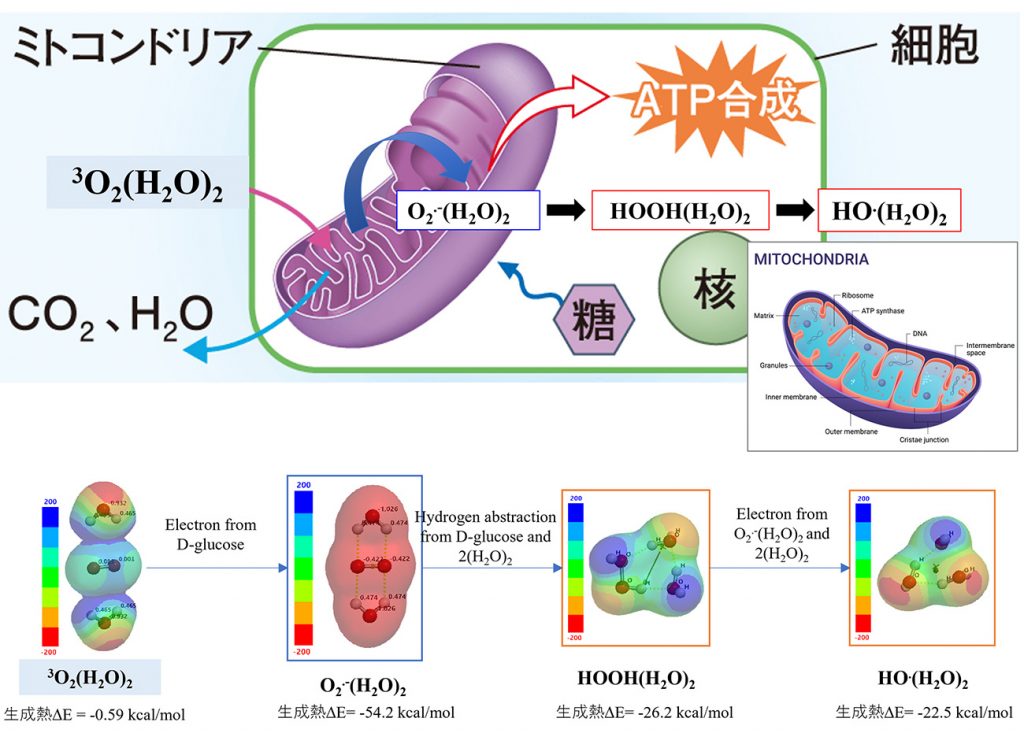
1. ミトコンドリア(mt)で発生する細胞の最初のエネルギー分子は、水和酸素[3O2(H2O)2]がD-グルコースによって還元されて生成する水和スーパーオキサイドアニオンラジカル[O2.-(H2O)2]である
ミトコンドリア(mt)で発生する分子種の平衡構造(静電ポテンシャルマップ(ESPM)表示)
2. O2.-(H2O)2は、エネルギー物質ATPを生産する一方、細胞内に水和過酸化水素[HOOH(H2O)2]として存在する
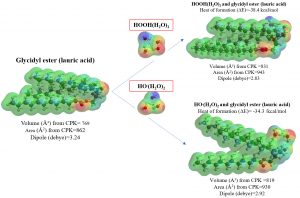
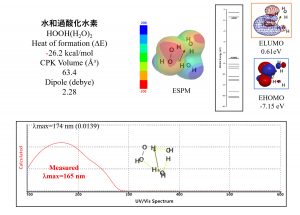
水和過酸化水素[HOOH(H2O)2]の存在の検証とvan der Waals 会合反応性を示す
表面静電ポテンシャルマップとエネルギー構造
水和スーパーオキサイドアニオンラジカル[O2.-(H2O)2]は、グルコースの水素原子を引き抜くと過酸化水素になる。HOOHはミトコンドリア中二分子の水和過酸化水素[HOOH(H2O)2]構造をとっている。このことは、DFT/MMで求めたFUV(下段に表示)が実測遠紫外吸収スペクトル(FUV)との一致に基づく。
[HOOH(H2O)2]のESPM構造の明確な青色赤色分布は、LUMO、HOMOの配座を反映、[HOOH(H2O)2]は様々な分子とvan der Waals 結合、すなわち、水素結合によって会合できることを検証する。
3. O2.-(H2O)2は、HOOH(H2O)2を還元して水和ヒドロキシルラジカル[HO.(H2O)2]を与えます。有酸素運動不足で細胞内でO2.-(H2O)2がATP生産等に消費されない場合起こる
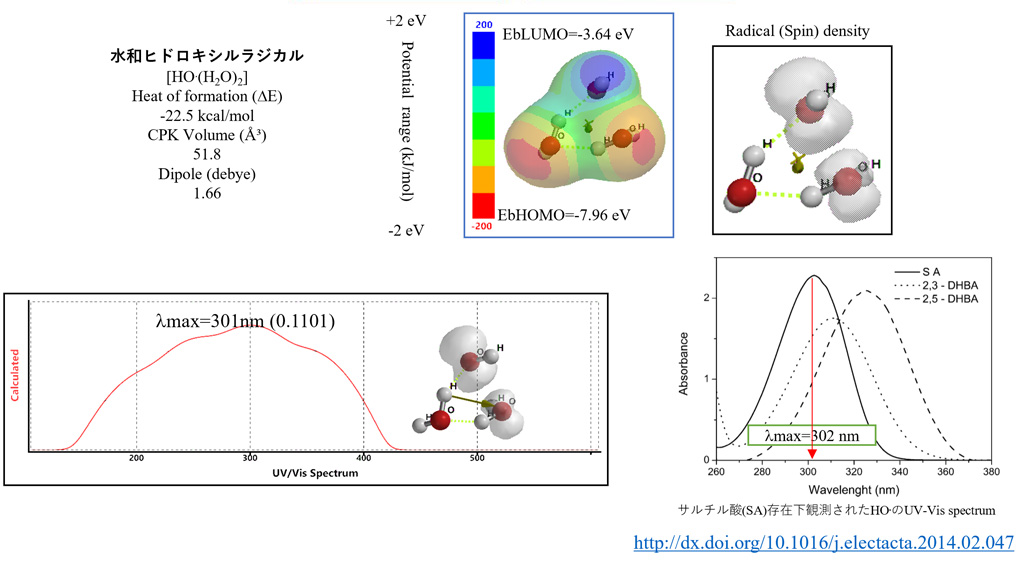
水和ヒドロキシルラジカル[HO.(H2O)2]の存在とその反応性の検証
ミトコンドリア(mt)細胞膜周辺で副生するHOOHのO2.-による還元によってヒドロキシルラジカルが発熱的に生じる(ΔE=-22.5kcal/mol)。その環状水和ヒドロキシルラジカル[HO.(H2O)2]の平衡立体構造を静電ポテンシャルマップ(ESPM)で表示した。[HO.(H2O)2]のDFT/MMに基づくUV-Vis spectrum(λmax=301nm)は、測定スペクトル(λmax=302nm)と一致した。このことは[HO.(H2O)2]の存在を検証する。
ESPM構造の青赤色の濃淡が顕著であることから、mt膜の親水表面とvan der Waals力(水素結合)で会合し易いことが理解できる。一方、ラジカル(スピン)(EbLUMO=-3.64 eV)はヒドロキシルラジカルの酸素上にあり、酸化的水素原子を引き抜き反応を検証している。
4. 水和ヒドロキシルラジカル[HO.(H2O)2]は、mtの脂質二分子膜を破壊してmtの細胞エネルギー(物質ATPと電磁波エネルギー)の生産代謝サイクルを破壊、細胞代謝を失速させる
悪玉活性酸素であるヒドロキシルラジカル[HO.(H2O)2]による
ミトコンドリアの脂質二分子膜の変形・破壊の検証
ミトコンドリア(mt)内で生じた過酸化水素[HOOH(H2O)2]はmtの脂質二分子膜上に吸着するが、膜構造に大きな変化をもたらさない。一方、[HOOH(H2O)2]からのヒドロキシルラジカル[HO.(H2O)2]がmtの脂質二分子膜上に吸着すると、mtの脂質二分子膜の配列に乱れを生じさせることが検証された。